揭秘直肠癌中BRAF“多样面孔”,思路迪诊断为临床治疗提供专业解读
2024-08-05 互联网在临床中,BRAF突变在结直肠癌中的发生率约8%-14%,而其中BRAF V600E是最常见的变异类型,与EGFR抑制剂的使用息息相关。如何看待检测出其它的变异类型?以及可能会遇到的非V600E变异有哪些?这些变异是否可以指导治疗?思路迪诊断团队结合长期科研成果,围绕临床中可能会遇到的非V600E变异情况,从多个角度进行分析解读,为相关临床治疗带来指导。
据介绍,BRAF基因所编码的BRAF蛋白,属于丝裂原活化蛋白激酶(MAPK)通路,通常称为 RAS-RAF-MEK-ERK信号级联。具有将上游信号传递至下游效应子以调节细胞增殖、分化、存活和死亡等生理过程的功能。作为人类癌症中最常见的突变信号通路,MAPK通路一直被认为是一种有前途的癌症治疗策略。RAF是MAPK通路的第一个蛋白激酶,具有三种亚型,即旁系同源物ARAF、BRAF 和 CRAF,具有高度相似的结构域组织。RAF 活化涉及一系列复杂的过程,包括从血浆中募集RAF、在膜中形成RAS-RAF复合物、RAF蛋白二聚化、RAF不同结构域的磷酸化或去磷酸化、与 RAF 激酶抑制蛋白分离以及与支架复合物如RAS激酶抑制因子结合。这些事件的确切顺序尚未得到很好的阐明,但RAF二聚化被广泛认为是关键步骤。RAF的三种亚型均能通过磷酸化激活MEK1/2,其中BRAF的活性最强。
在结直肠癌中,EGFR抑制剂被广泛应用于转化治疗和晚期治疗。其竞争性抑制EGFR细胞外配体,限制包括MAPK在内的异常细胞信号通路。BRAF的突变会直接激活MAPK信号通路,因此与EGFR抑制剂的耐药相关。但并不是所有BRAF突变的功能作用都一致,按照突变是否具有激酶活性、 激酶活性是否依赖于RAS活化以及BRAF是否需要二聚化,BRAF突变可分为三类(如图所示)。
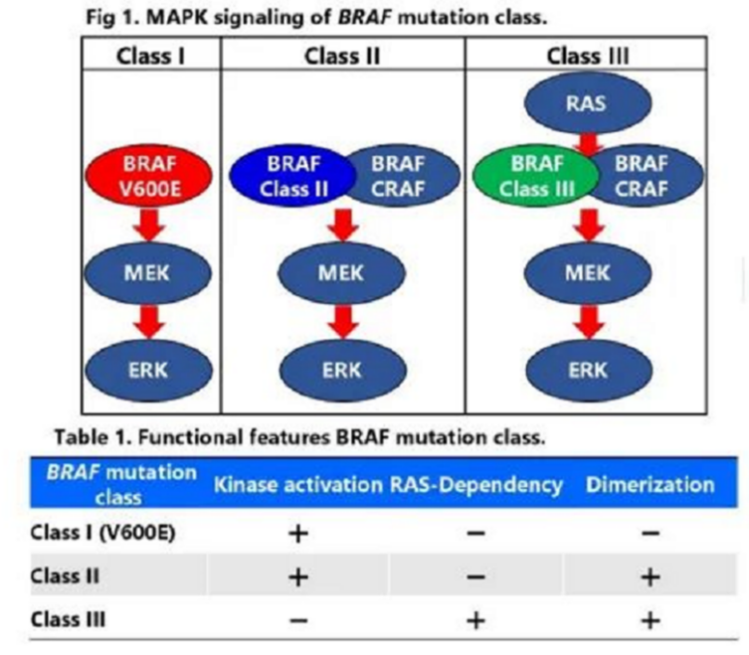
BRAF非V600E突变结直肠癌患者能考虑EGFR抑制剂吗?思路迪诊断科研团队在既往的NCCN指南研究中发现,对于EGFR抑制剂使用的限制条件之一是BRAF突变,而2024版NCCN指南则在脚注中新增提示“携带除V600E之外的BRAF突变的患者可考虑接受抗EGFR治疗”。这是因为,在结直肠癌中,不同的BRAF突变其实对EGFR抑制剂的敏感性不同。一项回顾性研究在40例非V600E BRAF突变转移性结直肠癌患者中分析对EGFR药物的应答,其中30%(12/40)为Ⅱ类突变,70%(28/40)为Ⅲ类突变。50%(14/28)的Ⅲ类突变和8%(1/12)的Ⅱ类突变患者接受抗EGFR疗法后产生了应答。Ⅲ类突变患者接受一、二和三线治疗后均观察到应答,但仅1例Ⅱ类突变一线治疗后观察到应答。
那么,如果基因检测检出BARF融合,应该怎样指导治疗?思路迪诊断专家表示,结直肠癌中,BRAF融合是一种罕见事件,检出率在0.3%-2.2%之间。而BRAF融合往往会导致N端CR1自抑制区域断裂,无法有效抑制BRAF活化,导致BRAF基因形成二聚体而结构性持续活化,这种功能类似于II类突变。例如AGAP3-BRAF(E1-9:E9-18)编码的融合蛋白包含BRAF的完整激酶结构域CR3,但缺少BRAF的CR1和CR2区。BRAF融合同样引起MAPK信号传导机制的激活,但影响程度不如BRAF V600E突变。
总体来说,BRAF变异除了常见的V600E之外,II类、III类突变以及BRAF融合仍然值得关注,检出BRAF基因变异并不代表着EGFR抑制剂的全盘否定,应及时确定具体的变异形式以辅助治疗方案的选择和预后情况的预测。要应对BRAF突变带来的一系列治疗难题,基础是全面掌握患者的基因变异信息。思路迪诊断取得的一系列科研创新成果显示,基于RNA的NGS更适合检测基因融合,结合两者优势进行DNA+RNA共检是最捷径之选,也是医学和科研界的共识。